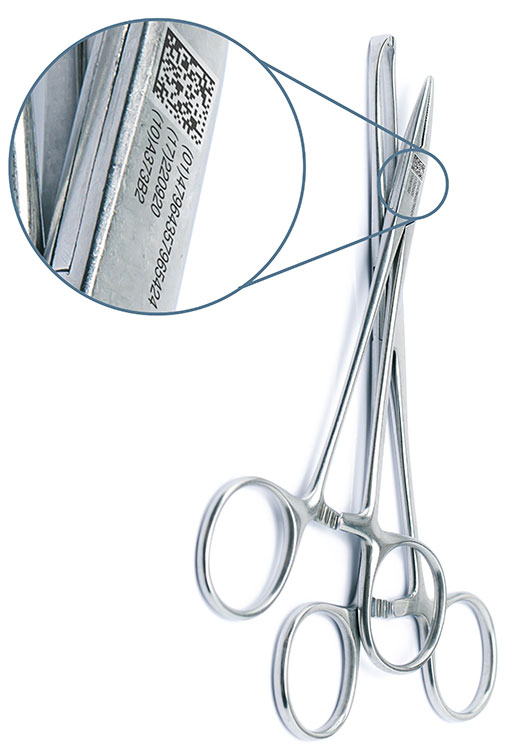
欧盟医疗器械法规 (MDR): 喷码要求和法规生效日期概览
MDR法规是适用于欧盟成员国的法规,对所有在欧盟内销售的医疗器械适用了严格的监管。2017年5月5日,欧盟医疗器械法规(REGULATION (EU) 2017/745,简称EU MDR)正式发布,并于2017年5月26日正式生效。欧盟委员会于2020年4月17日通过关于MDR实施日期推迟一年的建议,MDR生效日期推迟至2021年5月26日。
其中,新MDR法规提出将要求制造商为在欧盟境内分销的医疗器械标识名为唯一器械标识 (UDI) 的特定代码,即生产商需要严格执行在医疗器械以及其包装上进行UDI码打标和喷码的要求,对生产商以及标识行业者来说,这意味着包装流水线和标识设备技术都需要作出同步的转型和升级。
欢迎了解更多关于伟迪捷UDI码标识解决方案,或下载我们新的信息图表,了解更多关于UDI代码和不同医疗设备的风险等级。
联系我们
售前咨询: 400-920-2377
售后咨询: 400-886-8099